2021年05月,已重新向美国FDA提交了一份标签扩展申请,在降糖药Ozempic(诺和泰®,semaglutide,司美格鲁肽,皮下制剂,每周一次)的现有上市许可中,引入2.0mg的新剂量。
Ozempic是一款每周一次的胰高血糖素样肽1(GLP-1)类似物,该药是一种皮下注射制剂,目前在美国已批准0.5mg和1.0mg剂量,适用于:
(1)作为饮食调整和运动的辅助手段,以改善2型糖尿病成人患者的血糖控制;
(2)用于存在心血管疾病(CVD)的2型糖尿病成人患者,降低发生主要不良心血管事件(MACE,包括心血管死亡、非致死性心脏病发作、非致死性卒中)的风险。
在中国,诺和泰®(Ozempic,1.0mg,0.5mg)于2021年4月获得批准,用于治疗2型糖尿病(T2D)患者,改善血糖控制。诺和泰®是一款新型长效胰高糖素样肽-1(GLP-1)类似物,半衰期长达7天,适合每周注射一次且血药浓度平稳。兼具强效、长效和多效的诺和泰®,不仅将有效助力患者血糖平稳达标,并以全面心血管代谢获益帮助患者实现长久保护,大幅提高患者用药依从性,改善患者的生存质量,助力患者回归泰然生活。
semaglutide 2.0mg标签扩展申请,基于SUSTAIN临床项目中SUSTAIN FORTE试验的结果。这是一项为期40周的3b期疗效和安全性试验,共入组了961例需要强化治疗的2型糖尿病成人患者,评估了每周一次皮下注射semaglutide 2.0mg与semaglutide 1.0mg作为二甲双胍和/或磺脲类药物的补充。主要终点是:治疗第40周,血糖水平(HbA1c)的降低。
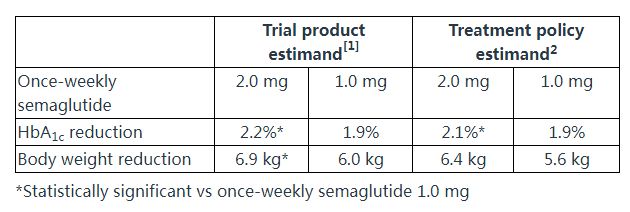
数据显示,试验达到了主要终点:在治疗第40周,2.0mg剂量组血糖水平(HbA1c)降低方面在统计学上显著优于1.0mg剂量组。此外,2.0mg剂量组在体重减轻方面也表现出优越性。
该试验中,2种剂量semaglutide均显示安全且耐受性良好。最常见的不良事件为胃肠道事件,大多数为轻至中度,随时间推移消失,与GLP-1受体激动剂类别一致。与1.0mg剂量semaglutide相比,2.0mg剂量semaglutide的胃肠道不良事件表现出相似性。
“海得康”发掘国际新药动态,为国内患者提供全球已上市药品的咨询服务,请咨询海得康医学顾问:400-001-9769,海得康官网微信:15600654560。


免责声明
由本文所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考,海得康不承担任何责任。
版权声明:本文为原创文章,版权归海德康海外医疗所有,转载请注明出处,感谢!
原创声明:如有侵权,请联系我们删除。

北京市经济技术开发区留学生创业园
科创十四街99号33幢D座7层703室
咨询热线:400-001-9763
Copyright @ 2017 北京海得康管理咨询有限公司 All Rights Reserved
互联网药品信息服务资格证(京)-非经营性-2016-0106
免责声明:本网站展示的医药信息仅供参考,具体疾病治疗和用药细节请务必咨询医生和药师,海得康不承担任何责任
京ICP备15058342号-15 工商执照注册号/统一社会信用代码 110105019927126

