溃疡性结肠炎是一种具有挑战性的疾病,许多患者仍然没有从最繁重的症状中获得缓解。这些阳性结果表明,在52周时,upadacitinib改善了临床、内镜和组织学结果。
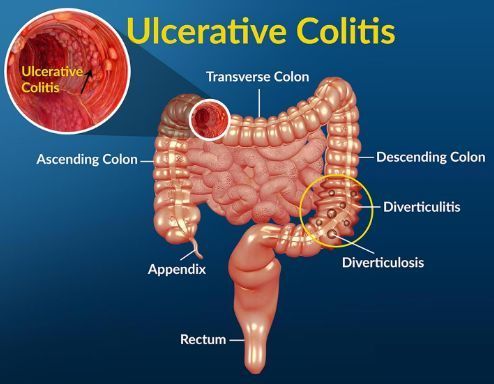
2021年6月,公布了口服JAK1抑制剂Rinvoq(upadacitinib,乌帕替尼)治疗中度至重度活动性溃疡性结肠炎(UC)的结果,数据显示,在第52周,该研究达到了全部次要终点,包括内镜改善、组织学内镜粘膜改善(HEMI)、无皮质类固醇临床缓解。具体数据为:
(1)在第52周,upadacitinib 15mg组、30mg组、安慰剂组分别有49%、62%、14%的患者达到内镜改善;
(2)在第52周,upadacitinib 15mg组、30mg组、安慰剂组分别有35%、49%、12%的患者达到HEMI;
(3)在完成8周诱导研究时处于缓解的患者中,在第52周,upadacitinib 15mg组、30mg组、安慰剂组分别有57%、68%、22%的患者达到无皮质类固醇缓解。
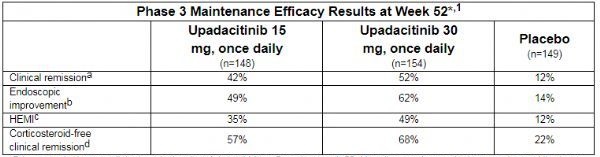
在52周研究期间,upadacitinib组中观察到的最常见不良事件是鼻咽炎、溃疡性结肠炎加重、血肌酸磷酸激酶水平升高。
Rinvoq是一种口服、每日一次的、选择性、可逆性JAK抑制剂。在欧盟,Rinvoq已被批准3个适应症:
(1)用于治疗对一种或多种疾病修饰抗风湿药物(DMARD)应答不足或不耐受的中度至重度类风湿性关节炎(RA)成人患者;
(2)用于治疗对一种或多种DMARD应答不足或不耐受的活动性银屑病关节炎(PsA)成人患者;
(3)用于治疗对常规疗法应答不足的活动性强直性脊柱炎(AS)成人患者。在这些适应症中,Rinvoq批准的剂量为15mg。
2021年06月,欧洲药品管理局(EMA)人用医药产品委员会(CHMP)发布一份积极审查意见,推荐批准Rinvoq(upadacitinib,乌帕替尼)一个新的适应症,用于治疗适合系统治疗的中度至重度特应性皮炎(AD)成人患者(15mg或30mg,每日一次)及12岁及以上青少年患者(15mg,每日一次)。

据海得康医学顾问了解到,乌帕替尼仿制药REMATIB已在孟加拉上市,由著名药企孟加拉耀品国际成功仿制,并获得孟加拉药监部门批准上市,所以质量有保障。患者如需用药,可自行出国就医。
“海得康”发掘国际新药动态,为国内患者提供全球已上市药品的咨询服务,请咨询海得康医学顾问:400-001-9769,海得康官网微信:15600654560。

乌帕替尼在全球多个国家已上市,海外药品上市情况,海外原研药/仿制药价格等,欢迎咨询海得康。

免责声明
由本文所表达的任何关于疾病的建议都不应该被视为医生的建议或替代品,请咨询您的治疗医生了解更多细节。本站信息仅供参考,海得康不承担任何责任。
版权声明:本文为原创文章,版权归海德康海外医疗所有,转载请注明出处,感谢!
原创声明:如有侵权,请联系我们删除。

北京市经济技术开发区留学生创业园
科创十四街99号33幢D座7层703室
咨询热线:400-001-9763
Copyright @ 2017 北京海得康管理咨询有限公司 All Rights Reserved
互联网药品信息服务资格证(京)-非经营性-2016-0106
免责声明:本网站展示的医药信息仅供参考,具体疾病治疗和用药细节请务必咨询医生和药师,海得康不承担任何责任
京ICP备15058342号-15 工商执照注册号/统一社会信用代码 110105019927126

